截至2021年3月15日,新型冠状病毒(SARS-CoV-2)已经造成全球1.2亿人感染,260万人死亡,这是本世纪最为严重的全球公共卫生事件。新冠病毒首先通过高度糖基化的刺突蛋白(S)上的受体结合域(RBD)与人类受体蛋白血管紧张素转换酶(ACE2)结合,进而侵袭人体细胞;因而糖基化的RBD也是疫苗与中和抗体的关键靶点。但由生物表达方法得到的RBD的糖链高度异质,可能影响以RBD为抗原的疫苗免疫原性以及造成不完整的抗体中和效果。通过高分辨质谱的手段已经,科学家已经完整解析病毒糖基化的位点以及糖型。然而,唯有获取含有特定均一结构糖型的蛋白质,才能够更为深入了解病毒糖基化的作用,有助于抗体药物研发以及疫苗设计。
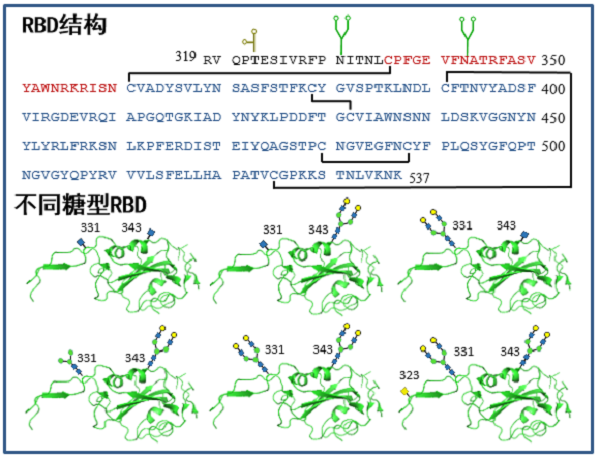
S-RBD由219个氨基酸组成(R319-K537),含有两个保守的N型糖基化位点(N331, N343)以及部分可能的O型糖基化位点(如T323),通过四对二硫键形成相应的三级结构。不同的生物表达体系以及人体内分离的病毒S蛋白上,糖链的结构均异常复杂。其中N331与N343主要由复杂型糖链构成,同时N331位点也有部分由N型糖链的核心五糖构成。相较于表达体系,化学合成糖蛋白具有精确的糖链结构,但其受限于冗长的合成路线。
近期,《德国应用化学》(Angewandte Chemie International Edition)在线发表了上海交通大学化学化工学院王平课题组最新成果“Synthetic Homogeneous Glycoforms of the SARS-CoV-2 Spike Receptor-Binding Domain Reveals Different Binding Profiles of Monoclonal Antibodies”。
上海交通大学王平团队结合蛋白质化学,糖化学和蛋白表达技术,发展了高效合成糖基化S-RBD的策略。在此基础上,高效大量合成了以单糖,核心五糖以及复杂型九糖为N型糖链(N331和N343),氨基半乳糖为O型糖链(T323)的六种不同糖型的RBD。S-RBD是目前人工合成最为复杂的糖基化蛋白之一。等离子共振实验表明,RBD糖基化的大小对其与ACE2的结合没有明显影响。与临床获批的中和抗体(S309, CB6等)结合力测试表明如抗体靶点为非糖基化区域,病毒糖基化造成的免疫逃逸效应不明显。在选择进化压力下,新冠病毒会改变糖型甚至糖基化位点来进行进化。该工作提供了一种高效大量制备均一糖链的S-RBD的平台,有助于更有效抗新冠病毒药物和疫苗的研发。同时,该合成平台也有助于对于其他冠状病毒(如SARS, MERS)的研究。
该研究工作获得国家自然科学基金,“生物大分子动态修饰与化学干预”重大研究计划和上海交通大学交叉学科专项资金等项目的资助。上海交通大学化学化工学院博士生叶发荣为本文的第一作者, 上海交通大学化学化工学院王平特别研究员为本文通讯作者。该工作也得到了中国科学院上海有机所俞飚,王婧研究员和复旦大学应天雷教授的大力支持。
论文信息:
Synthetic Homogeneous Glycoforms of the SARS-CoV-2 Spike Receptor-Binding Domain Reveals Different Binding Profiles of Monoclonal Antibodies
Farong Ye, Jie Zhao, Peng Xu, Xinliang Liu, Jing Yu, Wei Shangguan, Jiazhi Liu, Xiaosheng Luo, Cheng Li, Tianlei Ying, Jing Wang, Biao Yu, and Ping Wang
原文链接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202100543
原文引用:DOI:10.1002/anie.202100543

 English
English


